
Н.Ю. Серова, М.К. Тищенко, С.О. Никишов
ГБУЗ «Научно-исследовательский институт неотложной детской хирургии и травматологии»
Департамента здравоохранения, Москва
В статье представлены результаты сравнительного анализа лечения переломов костей голени у 102 детей в возрасте от 4 до 18 лет. Основную группу, в которой после оперативного лечения использовался метод пневматической имитации опорной нагрузки аппаратом «Корвит» на травмированную и здоровую нижние конечности, составил 51 (50%) пациент. В контрольную группу, в которой не применяли данный метод лечения, вошел 51 (50%) больной. Группы были сравнимы по возрасту, механизму и локализации травмы, методу оперативного вмешательства и комплексной терапии послеоперационного периода. В основной группе отмечены более ранние сроки уменьшения интенсивности болевого синдрома, отека мягких тканей, восстановления движений в смежных суставах и нормализация показателей соматометрии, что позволило раньше разрешить пациенту начать хождение и сократить сроки лечения.
Ключевые слова: дети, пневматическая имитация опорной нагрузки, перелом, кости голени, отек, методы фиксации.
The article contains a comparative analysis of shin fracture treatment in 102 children at the age of 4–18 years old. The main group consisted of 51 (50%) children, who received postoperative treatment according to the method of pneumatic imitation of weightbearing both on health and injured limbs with «Korvit» apparatus. The control group consisted of 51 (50%) patients who did not received the afore-mentioned method of postoperative treatment. The groups were comparable on age, trauma mechanism and localization, surgical operation and complex postoperative therapy. Children of the first group were found to have shorter period of time needed to achievement of pain relief, soft tissue swelling decrease, restoration of the movements in adjacent joints and somatometry values normalization, which allowed earlier verticalization and shorter period of hospitalization.
Key words: pneumatic imitation of weight-bearing, fracture, shin bones, swallowing, fixation methods, children.
ВВЕДЕНИЕ
Еще недавно в лечении переломов костей голени у детей превалировали консервативные методы. Однако скелетное вытяжение и гипсовая иммобилизация часто не позволяют добиться оптимальной репозиции и стабилизации отломков, на длительное время происходит обезд виживание поврежденной конечности и самого пациента. Консервативные методы лечения способствуют развитию функциональной недостаточности и мышечной гипотрофии поврежденной конечности, формированию постиммобилизационных контрактур смежных суставов и общей гиподинамии. Использование этих методов при переломах длинных костей, направленное сначала на сращение и лишь затем на восстановление функций конечности, затягивает сроки стационарного лечения, на длительный срок снижает качество жизни маленького пациента и его родителей, увеличивает время реабилитации до полного выздоровления ребенка [3–5]. Разработка и внедрение в клиническую практику систем внешней и внутренней фиксации для стабилизации костных отломков позволили значительно сократить сроки лечения больных с травмами опорно-двигательного аппарата, быстрее восстанавливать функциональность конечности. Однако конструкции внешней фиксации громоздки, требуют постоянного ухода, и нередко их применение осложняется воспалением окружающих тканей и/или прорезыванием спиц. Открытые оперативные методы лечения позволяют добиться прочной и точной фиксации отломков и приводят к дополнительному повреждению мягких тканей, осложнениям, косметическим дефектам [6, 7].В настоящее время показатели детского травматизма превышают таковые у взрослых пациентов. Из общего числа повреждений большая часть приходится на травмы опорно-двигательного аппарата. Переломы костей голени у детей являются наиболее частыми повреждениями скелета и составляют от 15 до 20% всех переломов опорно-двигательной системы [1, 2], что совпадает с данными нашего института в период с 2007 по 2011 гг.
В настоящее время отработана хирургическая техника миниинвазивного металлоостеосинтеза (ММОС) [2, 7]. В лечении переломов костей голени используют такие фиксаторы, как TENы — гибкие титановые штифты, LCP — блокируемая компрессирующая пластина, UTN — интрамедуллярные блокируемые гвозди, компрессирующие винты и Hcs (канюлированные) винты. Преимуществами ММОС по сравнению с классическими методами являются минимальная травматичность, отсутствие необходимости в оперативном доступе в зоне перелома, оптимальная репозиция и стабилизация отломков при отсутствии внешней иммобилизации. Современные технологии позволяют использовать аппаратные методики и являются принципиально важным подходом в комплексном лечении, т. к. они сохраняют и поддерживают функции поврежденной конечности уже с первых сут после оперативного лечения [2, 3, 7]. Ультразвуковое исследование мягких тканей и костей дает возможность уточнить характер и степень повреждения и смещения отломков, а также циркуляцию в магистральных сосудах и в зоне образования костной мозоли [8, 9]. Однако в научной литературе нет описания методик соматометрического и эхографического исследования в динамике при переломах костей голени у детей. блем, пневматический имитатор опорной нагрузки, воздействуя путем стимуляции опорных зон и проприорецепторов, по данным функциональной магнитно-резонансной томографии, формирует афферентный поток импульсов, который оказывает регулирующее действие на контролирующие движения структуры центральной нервной системы, такие как первичные моторные области и дополнительные зоны активации (первичная сенсорная кора, поля Бродмана, нижние отделы постцентральных извилин, парацентральные дольки, области верхних и нижних теменных долей, дорсолатеральные префронтальные области коры), отвечающие за выполнение сложного локомоторного акта — шага и ходьбы [12]. Специальных исследований, посвященных разработке и оценке комплексного лечения переломов костей голени у детей с использованием аппаратных методик на ранних сроках послеоперационного периода, в доступной литературе мы не встретили.
Цель работы: оценить эффективность комплексного лечения переломов костей голени у детей, оперированных по малоинвазивным методикам металлоостеосинтеза, с применением метода ПИОН в раннем послеоперационном периоде.
ПАЦИЕНТЫ И МЕТОДЫ
В исследование были включены 102 ребенка в возрасте от 4 до 18 лет, поступившие в НИИ НДХиТ за период с 2010 по 2012 гг. для хирургического лечения по поводу переломов костей голени. Из общего числа детей 40 (39%) — девочки и 62 (61%) — мальчики. Половина пациентов составила основную группу, в которой помимо общепринятого комплексного лечения применялась аппаратная имитация опорной нагрузки, 51 (50%) — контрольную группу. Обе группы были сопоставимы по возрасту, полу, механизму и локализации травмы, срокам и методу оперативного вмешательства, виду фиксаторов. Дети были распределены на 4 возрастные группы: 1-я — от 4 до 6 лет, 2-я — от 7 до 10, 3-я — от 11 до 14, 4-я — от 15 до 18. Большая часть наблюдаемых были пациентами 3 и 4-й возрастных групп. Средний возраст больных составил 12 лет 6 мес ± 2 года 4 мес (табл. 1).
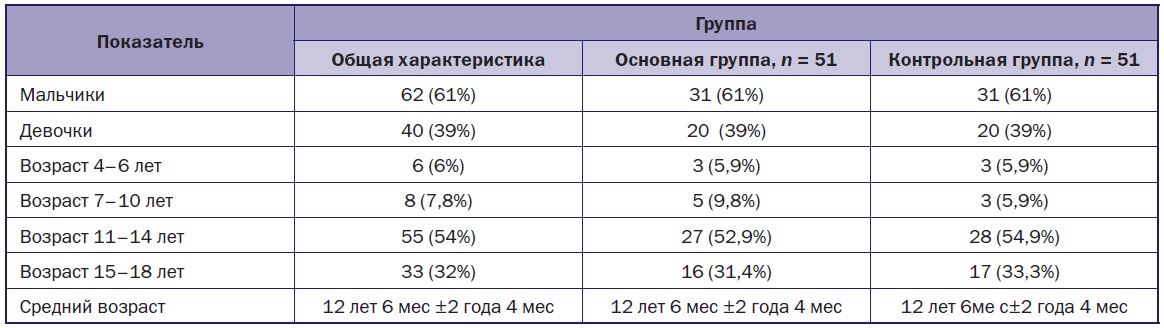
Таблица 1. Сравнение пациентов по полу и возрасту
Уличный травматизм стал причиной перелома у 58 (57%) детей, спортивный, в т. ч. полученный на уроке физкультуры, — у 20 (19,6%), дорожный — у 14 (13,7%), бытовой — у 10 (9,7%). Диафизарный перелом костей средней трети голени был диагностирован у 26 (25,5%) человек, диафизарный перелом костей нижней трети голени — у 10(9,7%), метаэпифизеолиз дистального отдела большеберцовой кости — у 31 (30,4%), перелом передненаружного отдела большеберцовой кости — у 17 (16,7%), двухлодыжечный перелом — у 4 (4%), перелом медиальной лодыжки — у 11 (10,8%), эпифизеолиз дистального отдела большеберцовой кости — у 3 (2,9%). Закрытые переломы составили основную часть переломов — у 98 (96%) пациентов, открытые — лишь у 4 (4%). Перелом одной кости голени был диагностирован у 60 (59%) детей, обеих костей голени — у 42 (41%). Изолированные переломы диагностировали у 92 (90%) детей, повреждение конечности с явлениями неврита имело место у 4 (4%), сочетанная травма — у 5 (4,9%): закрытая черепно-мозговая травма, сотрясение головного мозга — у 4, компрессионный перелом позвоночника — у 1 (табл. 2).
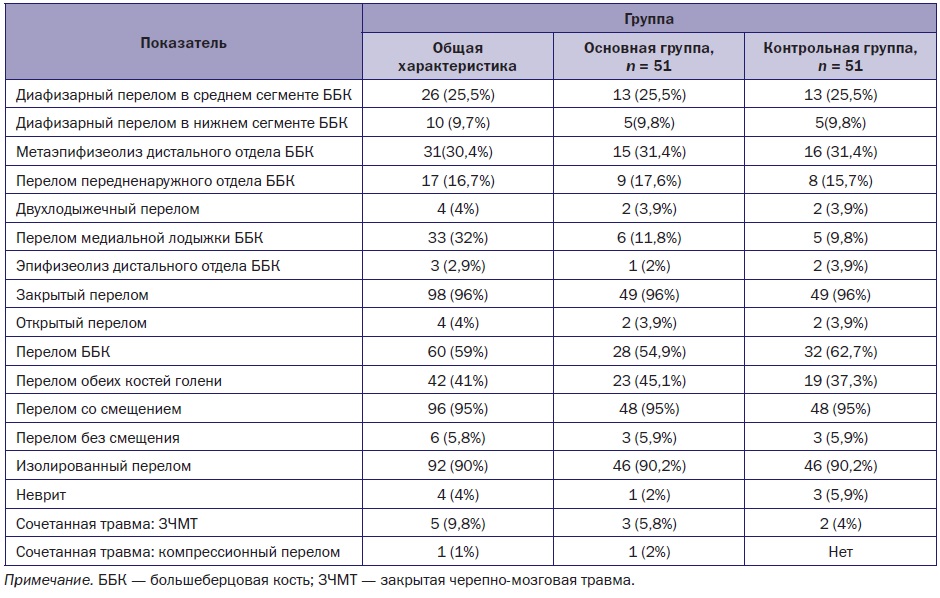
Таблица 2. Сравнение детей по характеристикам перелома
В общей структуре преобладали переломы со смещением — у 86 (84%) наблюдаемых. Большинство детей (76–75%) поступили в первые сутки после травмы и были прооперированы в срочном порядке. Скелетное вытяжение как основной метод лечения не применяли, он был использован с целью первичной иммобилизации у 15 (16%) пациентов в периоде, предшествующем оперативному вмешательству, длительностью от 1 до 5 суток. Всем больным был выполнен ММОС, во всех случаях отсутствовала наружная иммобилизация или аппаратная внешняя фиксация: 86 (84%) пациентам выполнено закрытое реконструктивное малоинвазивное оперативное вмешательство, 16 (16%) — открытое. При лечении указанных повреждений использовали различные фиксаторы ММОС: компрессирующие винты установили 38 (37%) детям, винты Hcs — 29 (28%), в том числе с дополнительной фиксацией малоберцовой кости спицей — 9 пациентам, LCP — 12 (12%), UTN — 12 (12%), TENы —11 (11%). Больным основной и контрольной группы назначили однотипное лечение (табл. 3).
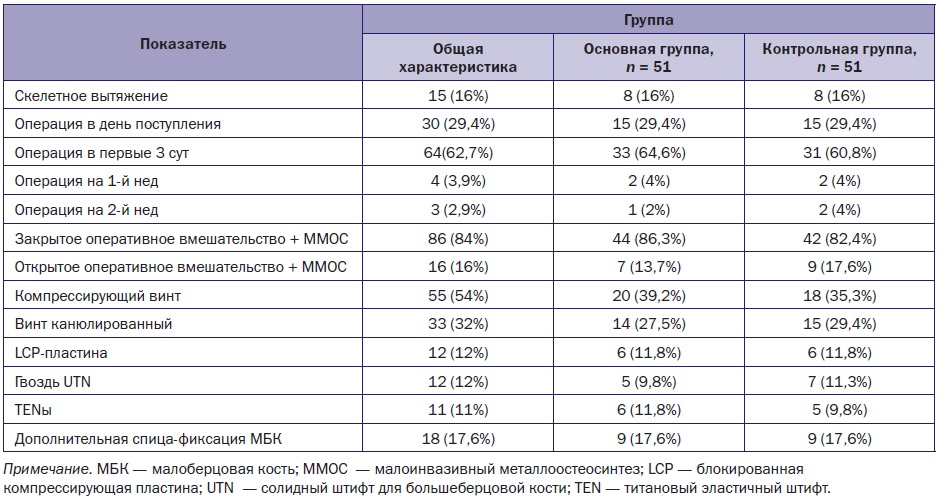
Таблица 3. Сравнение лечения в основной и контрольной группах
Оценку эффективности применения методики ПИОН осуществляли по числовой, вербальной аналоговой либо (у детей с 4 до 8 лет) мимической шкале болевого синдрома от 0 до 10 с помощью соматометрии (амплитуда движений, отечность конечности) и ультразвукового исследования.
Соматометрический контроль включал измерение длины окружности обеих конечностей в симметричных областях, измерение объема и амплитуды движений в голеностопных суставах. Полученные показатели сопоставляли, суммировали и сравнивали с показателями для здоровой конечности, которые принимали за норму.
Ультразвуковое исследование выполняли после операции на аппаратах экспертного класса «SonoSite MicroMaxx» (SonoSite Inc., США), сравнивая травмированную конечность со здоровой, оценивая повреждения, толщину мягких тканей голени, измерение и описание m. Tibialis anterior на сроках 1, 6, 10-е сутки и после разрешения опорной нагрузки, на 60-е сутки со дня оперативного вмешательства.
Контрольные осмотры после выписки проводили через 3–4 нед, 45 дней и 2 мес после установки металлоконструкции. Результаты оценивали по нескольким параметрам: срокам вертикализации, нормализации размеров конечности и срокам начальной консолидации переломов.
Компьютерный анализ фактических данных осуществляли в программах Microsoft Excel XP и SPSS Statistics 17.0 с использованием мультифакторного дисперсионного анализа показателей в динамике и t-критерия равенства средних значений для оценки результатов лечения. Различия считали достоверными при p < 0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Каждый ребенок основной группы с первого послеоперационного дня получал процедуры ПИОН с помощью аппарата модели «Корвит» (регистрационное удостоверение № ФСР 2009/04901 от 25 мая 2009 г.) продолжительностью 10 мин. В первый послеоперационный день давление в пневматических подушках устанавливали на минимальном уровне (10 кПа). С целью максимально быстрого восстановления функции поврежденной конечности авторами разработана методика проведения ПИОН. С первых суток после оперативного вмешательства режим ходьбы устанавливался дифференцировано. У детей младшего возраста (до 6 лет) — 8 процедур по 10 мин с давлением 10–20 кПа в режимах «медленной ходьбы» (75 циклов в минуту, ц/мин; длительность шага 800 мс) либо «средней ходьбы» (120 ц/мин, 500 мс), либо «быстрой ходьбы» (150 ц/мин, 400 мс). У детей старше 6 лет — 8 процедур по 10 мин с давлением 20–30 кПа в режимах «средней ходьбы» (120 ц/мин, 500 мс) либо «быстрой ходьбы» (150 ц/мин, 400 мс). Дети охотно принимали процедуры ПИОН, которые не вызывали у них негативной реакции вследствие безболезненности и отсутствия каких-либо неприятных ощущений в процессе проведения. При этом мог сохраняться игровой элемент в общении. У 47 (93%) пациентов основной группы отмечено уменьшение интенсивности болевого синдрома, исчезновение страха движения в смежных суставах, снижение отечности конечности. Лечебный эффект был очевиден, когда уменьшался болевой синдром, поскольку отсутствие боли позволяло детям заниматься лечебной физкультурой активнее по сравнению с пациентами контрольной группы (табл. 4, рис. 1).
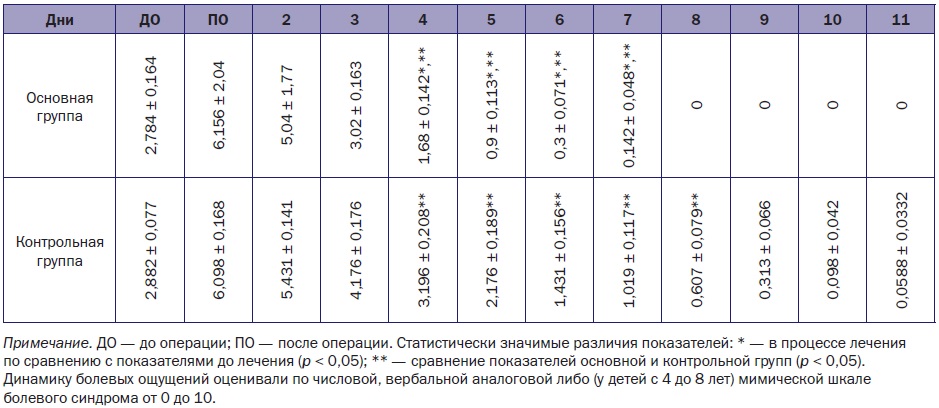
Таблица 4. Динамика болевого синдрома
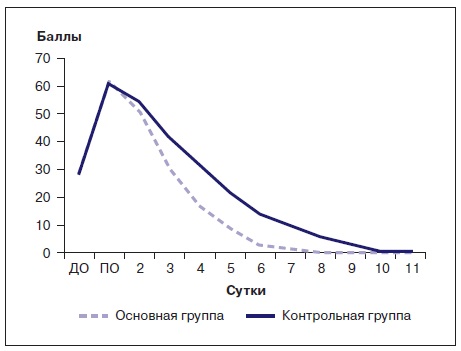
Рис. 1. Динамика болевого синдрома
Сравнение обеих групп в день операции, после нее, на 1-е и 2-е сутки не показало достоверных отличий. Разница измерений показателей поврежденной конечности по сравнению со здоровой на момент оперативного вмешательства у основной группы составила 9,18 ± 0,68 см, у контрольной — 9,4 ± 0,6; после операции — 8,92 ± 0,68 и 9,19 ± 0,64 см, соответственно; нарастала в 1-й день после операции (10,5 ± 0,67 и 11,19 ± 0,62).
Таким образом, есть основания говорить о том, что по тяжести полученной травмы и величине отека основная и контрольная группы были сопоставимы. Однако, начиная со 2-х суток отмечено значимое отличие между показателями обеих групп. К 5-м суткам соматометрический показатель разницы измерений поврежденной конечности по сравнению со здоровой в основной группе составил 6,35 ± 0,57 см, в контрольной — 9,11 ± 0,59, а по сравнению с исходными данными в динамике были установлены достоверно различающиеся показатели уменьшения степени выраженности отека в основной группе (p < 0,01). К моменту выписки из стационара у пациентов основной группы разница сумм измерений составила 2,18 ± 0,4. Не отмечено и нарастания отека в течение последующих суток; те же показатели на контрольном осмотре на 30-е сутки составили (–0,27) ± 0,19, а на 60-е сутки — 0,15 ± 0,11. В контрольной группе отек продолжал сохраняться и на 10-е сутки (3,56 ± 0,47), поврежденная конечность была изменена и после выписки из стационара — (–1,43) ± 0,36, у нее присутствовали признаки гипотрофии. Отек конечности у пациентов контрольной группы был диагностирован и после назначения опорной нагрузки в течение 3 недели (1,02 ± 0,34). Динамика изменений степени выраженности отека и объема движений у пациентов основной и контрольной группы представлена в табл. 5 и на рис. 2, 3.
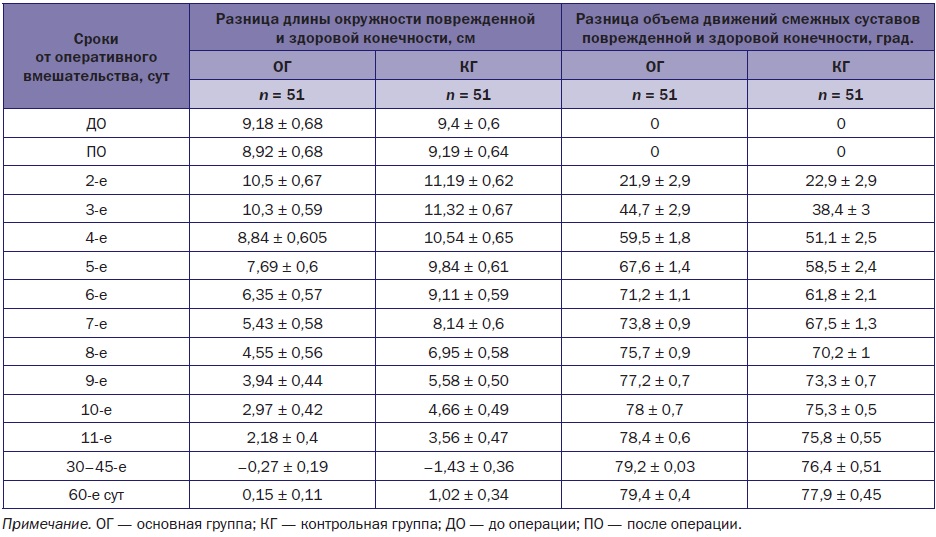
Таблица 5. Динамика соматометрических показателей здоровой и поврежденной конечности
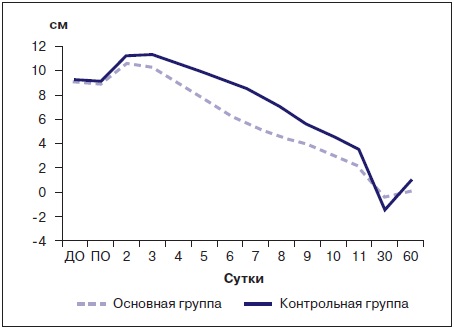
Рис. 2. Динамика соматометрических показателей здоровой
и поврежденной конечности
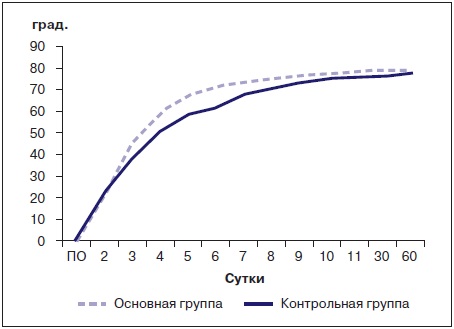
Рис. 3. Сравнение амплитуды движений в голеностопном
суставе
Согласно данным ультразвукового контроля, проявление отека и изменения структурности m. Tibialis anterior у пациентов основной группы носили транзиторный характер, тогда как в контрольной группе они сохранялись в течение длительного периода времени. На 1-е сутки после оперативного лечения показатели разницы толщины мягких тканей поврежденного сегмента по сравнению с симметричным участком здоровой конечности составили в обеих группах 0,55 ± 0,04 см (основная и контрольная группа сопоставимы в начале лечения), на 6-е сутки — 0,47 ± 0,39 и 0,54 ± 0,04, на 10-е сутки — до 0,35 ± 0,03 и 0,44 ± 0,03 см, соответственно. Такое состояние наблюдаемых сохранялось на контрольном эхографическом исследовании на 60-е сутки после перелома, т. е. спустя 3 неделю после назначения опорной нагрузки: 0,16 ± 0,01 в основной группе и 0,38 ± 0,03 см в контрольной. Подобные изменения происходили с m. Tibialis anterior в динамике. Изменения степени выраженности отека по данным ультразвукового исследования пациентов основной и контрольной групп представлены в табл. 6, 7 и на рис. 4, 5. В целом снижение величины отечности в динамике при применении ПИОН «Корвит» в комплексном лечении у пациентов основной группы оказалось статистически значимым (p < 0,01).
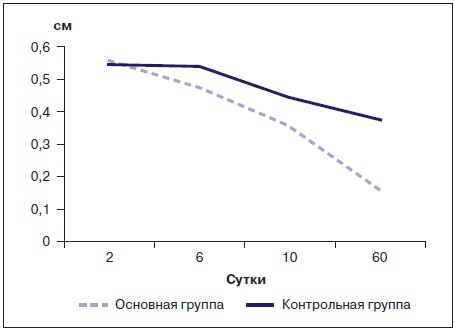
Рис. 4. Сравнение соматометрических показателей в динамике
по данным ультразвукового исследования
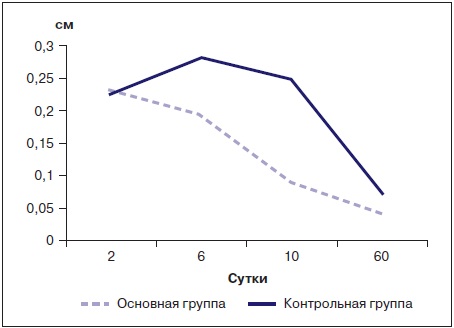
Рис. 5. Сравнение толщины m. Tibialis anterior в динамике
по данным ультразвукового исследования
Оценку результатов лечения проводили по 3 параметрам. Вертикализация пациентов в основной группе происходила, по средним данным, на 1,62 ± 0,09 сутки, тогда как в контрольной группе — на 2,12 ± 0,11 (p < 0,01). Нормализация размеров конечностей в основной группе — на 26,94 ± 2,53 сутки, в контрольной — на 42,29 ± 2,82 (p < 0,01). Сроки проявления начальной консолидации на контрольных рентгенограммах в динамике после выписки из стационара составили 41,76 ± 1,21 сутки в основной группе и 51 ± 1,54 — в контрольной (p < 0,05), данные представлены в табл. 8. Таким образом, можно утверждать, что у детей, получавших лечение с применением ПИОН «Корвит», улучшилось общее самочувствие и функциональные возможности поврежденной конечности, поддерживался тонус мышц поврежденной конечности, повышалась общая двигательная активность и происходил ранний перевод с постельного режима на общий.

Таблица 6. Сравнение соматометрических показателей в динамике по данным ультразвукового исследования

Таблица 7. Сравнение толщины m. Tibialis anterior в динамике по данным ультразвукового исследования

Таблица 8. Результаты лечения детей основной и контрольной групп
Применение указан ной методики способствует раннему восстановлению ходьбы за счет сохранения опороспособности, что достигается путем поддержания функционального состояния связочно-мышечного аппарата поврежденной нижней конечности. Осложнений или отрицательного воздействия у пациентов не наблюдалось. Осевая нагрузка была разрешена через 1 месяц: дети практически сразу начали ходить без хромоты и уже через несколько дней могли посещать детские учреждения.
У 28 пациентов контрольной группы жалобы на отек, хромоту сохранялись до 2 месяцев, отмечалась гипотрофия поврежденной конечности при наличии отека мягких тканей по результатам ультразвукового исследования.
ЗАКЛЮЧЕНИЕ
Предложенные методики оценки поврежденной конечности по соматометрическим показателям и эхографического мониторинга у детей с переломами костей голени, оперированных по ММОС, позволяют объективизировать характер и степень повреждения, в динамике проследить за изменениями тканей. Согласно усовершенствованной методике проведения процедур, аппаратную ПИОН целесообразно использовать с первых суток после оперативного вмешательства. Режим ходьбы определяется дифференцировано.
Установлена прямая связь соматометрических и эхографических показателей в зависимости от времени послеоперационного течения и применения ПИОН. Использование аппарата в раннем послеоперационном периоде не оказывает негативного воздействия, ускоряет репаративные процессы. Показатели соматометрических измерений, объема движений и ультразвукового обследования свидетельствуют об эффективности процедур и более ранней активизации пациентов (с первых суток после оперативного вмешательства).
Таким образом, включение ПИОН в комплексное лечение переломов костей голени у детей улучшает результаты лечения, сокращая сроки восстановления, облегчая состояние пациента. Применение настоящей методики в раннем послеоперационном периоде у детей с переломами костей голени может быть рекомендовано для использования в специализированных лечебных учреждениях.
СПИСОК ЛИТЕРАТУРЫ
1. Быков В. М., Ковшова М. Ф., Горшенина О. В. Конф. детских травматологов-ортопедов России «Актуальные вопросы детской травматологии и ортопедии»: Сб. тезисов. М. 2001. 327 с.
2. Крикунов А. И., Пужицкий Л. Б. Выбор метода фиксации переломов обеих костей голени у детей. Детская хирургия. 2011; 3: 22–24.
3. Петров А. Г., Акинфиев А. В. Экстракортикальный остеосинтез при лечении диафизарных переломов длинных трубчатых костей у детей старшего возраста. Казань: ИД «Практика». 2009. 16 с.
4. Чукина Е. А. Комплексное восстановительное лечение больных с переломами дистального отдела костей голени и лодыжек. Автореф. … дис. канд. мед. наук. М. 1997.
5. Xiao M., Li J., Zhang X., Zhao Z. Factors affecting functional outcome of Sichuan-earthquake survivors with tibial shaft fractures: a follow-up study. J. Rehabil. Med. 2011; 43 (6): 515–520.
6. Мельцин И. И. Дифференцированный металлоостеосинтез при диафизарных переломах длинных трубчатых костей у детей. Автореф. дис. … канд. мед. наук. М. 2009.
7. Пужицкий Л. Б., Ратин Д. А., Никишов С. О. и др. Малоинвазивный металлосинтез у детей. MargoAnterior. 2009; 3: 10–12.
8. Синицина Н. В., Ватолин К. В., Выборнов Д. Ю. и др. Ультразвуковая диагностика репаративного остеогенеза при переломах длинных трубчатых костей предплечья у детей. Детская хирургия. 2010; 3: 14–17.
9. Cross K. P. Прикроватное ультразвуковое исследование переломов трубчатых костей у детей. Clin. Ped. Еmerg. Med. 2011;12 (1): 27–36.
10. American Academy of Orthopedic Surgeons. Study for the new clinical guidelines of leg fractures in children.
11. Чухлина У. А., Щепкина В. А., Клювкин И. Ю. и др. Опыт использования прерывистой пневмокомпрессии на раннем этапе лечения больных с переломами нижних конечностей. Физиотерапия, бальнеология и реабилитация. 2010; 3: 14–17.
12. Хунустдинова Д. Р. Роль опорной афферентации в поддержании скоростно-силовых свойств и выносливости антигравитационных мышц. Автореф. … дис. канд. мед. наук. М. 2007.



